随着靶向治疗在近年来的迅猛发展,凭借着高效低度的优势,靶向治疗在肿瘤治疗当中的主体地位已经确立。作为靶向治疗与生俱来的缺陷,即耐药性,在制约靶向治疗发展的同时,也给靶向治疗带来了新的方向与思路。作为目前靶向治疗中最为成熟的治疗模式,即以针对晚期非小细胞肺癌EGFR突变的靶向治疗,在经历了第一代靶向药物的漫长旅程,第二代靶向药物的反响平平以及第三代靶向药物的高歌猛进之后,肺癌的靶向治疗再次成为全球的焦点。而这一切很可能归功于民间所谓的针对EGFR突变第三代小分子靶向神药AZD9291(osimertinib,奥希替尼)在全球的获批1。事实上,不管从疗效还是从全球审批进度来讲,AZD9291的成名之路让我们觉得有点不可思议。然而当我们惊叹于AZD9291神奇的疗效与较低的毒副反应的同时,AZD9291所带来的耐药性问题就好比是往这场欢庆的party上泼了一瓢冷水。
从耐药机制上来看,AZD9291的耐药大致可分为EGFR依赖型与EGFR非依耐型两类2。这种分类对治疗参考的意义就在于针对EGFR治疗的潜力是否还能继续挖掘。因为从临床观察角度来讲,在经历了第一代靶向药物如erlotinib,icotinib
,gefitinib的耐药之后,继续使用第3代靶向药物如AZD9291后出现耐药的患者的生存期基本上都是在2年以上,属于晚期肺癌治疗中的优势人群。考虑到目前第4代的药物如EAI045尚处于临床前研究阶段,使用单一的药物来破解AZD9291所引起的耐药显然不太现实,联合治疗似乎更为合理,afatinib
或者brigatinib
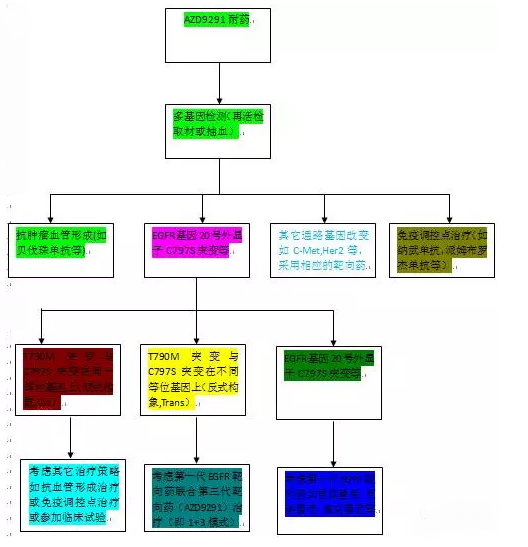
联合cetuximab即为代表性的例子。另外,之所以反复强调将EGFR进行到底是因为从肿瘤异质性的角度来讲,即使是真的出现耐药,仍然有一部分细胞对AZD9291比较敏感,突然停药的话,肿瘤有可能出现反弹。而从肿瘤进展模式的角度来考虑,在临床中有相当一部分患者其实是可以继续加量口服AZD9291,尤其是出现脑转移或者脑膜转移,同时采取联合局部治疗手段如放疗,手术等方式来进一步控制肿瘤。但是从精准医学的角度来讲,这种大致的分类有点模糊不清,尤其是在近年来ctDNA技术与NGS技术的推动下,使用这些新的手段能够进一步检测靶向药物的耐药改变,从而进一步根据基因改变进行分类,其标本来源不止可以使用组织,而且可以通过抽血来实现。尽管很多时候,检测得到的结果五花八门,但是从处理模式大致来讲,得到的结果也就是yes
or
no,当中所谓的yes是指找到可针对的靶点,而no则表示没有找到靶点或者尽管有靶点被鉴别出来,但是目前尚无相应的药物。对于前者,自然可以继续使用相应的靶向药物来进行处理,如出现Her2扩增可采用herceptin,出现C-Met扩增可考虑联合crizotinib
or
cabozantinib等3。而对于后者,靶向治疗的道路似乎已经走到了尽头,但是考虑到目前肺癌中已有的其它治疗模式,如免疫调控点治疗4以及抗血管生成治疗5,这部分患者依然还是有很大的治疗空间,对这部分患者使用合理的药物联合有时也能在临床上取得意想不到的效果,这时候也是考验临床医生水平的时候了。不可否认,多靶点筛查在寻找克服耐药策略方面确实起到了投石问路的作用,但是太多的线索有时也会对临床造成干扰。这个时候,对靶向药物的选择可能不应当只局限于AZD9291耐药之后的靶点改变,而应当回到原点如最初的EGFR突变状态,即通常的EGFR
19号缺失与21号外显子的L858R突变,因为从目前已经发表的数据来看,这两种突变类型的患者使用AZD9291的结局并非完全一致,即使是使用AZD9291之后出现相同的耐药突变,其处理策略以及预后也大相径庭,换句话来讲,也就是精准精准再精准的时候了6。
综上所述,尽管目前通过新的检查手段筛查出耐药改变从而采用相应的靶向药物或者使用新的药物组合能够从一定程度上克服克服AZD9291的耐药性,但是,考虑到AZD9291正式进入临床的时间不足2年,这些策略目前很多要么停留在理论水平,要么缺乏高级别的临床研究证据支持,AZD9291的耐药性的克服将会是未来肺癌治疗的新的难点,重点与热点。而随着检测手段与靶向治疗的日渐成熟,同其先辈gefitinib一样,AZd9291的耐药性也将被克服,从而使肺癌的靶向治疗继续向前向前。